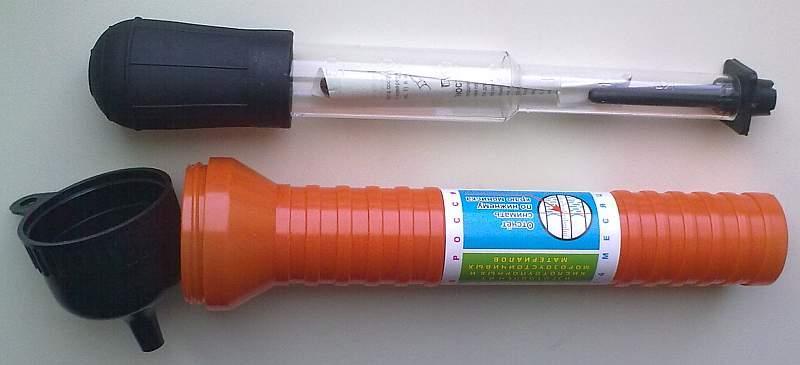
Какая кислота используется в аккумуляторе автомобиля
Содержание:
Применение серной кислоты и её сорта
Вообще, в качестве электролита в некоторых видах автомобильных аккумуляторов может использоваться щёлочь. Например, никель-кадмиевый или никель-железный тип АКБ. Есть ещё группа гелевых аккумуляторов AGM и GEL, где электролит находится в связанном состоянии. Но это тот же раствор серной кислоты. Просто он либо переведён в гелеобразное состояние с помощью добавок (GEL), либо им пропитано стекловолокно (AGM). Наиболее распространёнными на сегодняшний день остаются свинцово-кислотные автомобильные аккумуляторы с жидким электролитом. Поэтому речь пойдёт именно о водном растворе серной кислоты, предназначенном для заливки в АКБ.
Существуют основные сорта серной кислоты, которые перечислены ниже:
Порядок заливки и доливки кислотного электролита в АКБ
Составляющие компоненты электролита – кислоту и дистиллированную воду, нужно смешать в разных пропорциях. Так, если необходимо получить электролит с уровнем плотности 1,29 г/см³, то к 1 литру необходимо добавить 0,36 л кислоты, то есть в соотношении 1:3.
Заливку электролита производят стеклянной или полиэтиленовой трубочкой до уровня 10-15 мм над свинцовыми пластинами. После этого аккумулятор оставляют на два часа, однако в некоторых случаях плотность при этом падает. Далее АКБ заряжают током в десять раз меньшим его емкости в течение 4 часов.
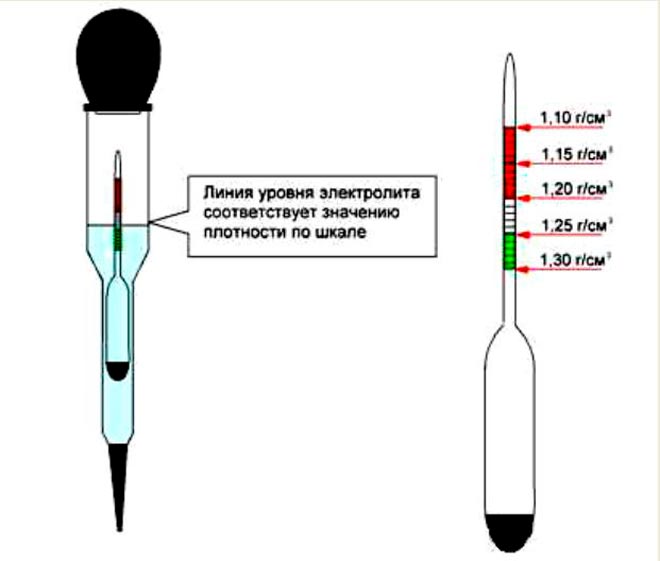
Проверять плотность АКБ необходимо раз в 2-3 месяца. Для этого используется специальный прибор – ареометр.
Важно! В целях техники безопасности необходимо знать, что заливать нужно именно серную кислоту в дистилированную воду, но не наоборот, поскольку высока вероятность возникновения химической реакции данной смеси с выделением брызг и тепла
Что такое ацидоз и алкалоз
Чтобы обеспечить нормальное функционирование метаболических процессов и снабжение тканей достаточным количеством кислорода, нормальный pH крови должен поддерживаться в узком диапазоне 7,36-7,44.
- Ацидоз – это состояние с избытком кислот в крови, что приводит к падению pH крови ниже 7,36.
- Алкалозом называют избыток оснований в крови с последующим повышением pH крови выше 7,44.
Повлиять на регулирование pH крови и привести к тому, что pH крови окажется за пределами диапазона здоровых людей могут многие состояния и заболевания. Равновесие можно восстановить, увеличив выведение и / или уменьшив потребление этих веществ.
Определение ацидоза и алкалоза
Электролит
Электролит для свинцовых батарей представляет собой водный раствор серной кислоты. Серную кислоту и дистиллированную воду применяют с вышеуказанными характеристиками. Для заливки новых стационарных АКБ и вышедших из ремонта, а также для доливки применяется электролит с плотностью 1,18-1,24 г/см3.
Если для приготовления электролита применяется серная кислота с плотностью 1,83 г/см3 — целесообразно работы вести в два этапа. На первом этапе готовится электролит с плотность. 1,4 г/см3. Необходимо обеспечить его остывание до температуры 20С. На втором этапе из электролита с плотностью 1,4 г/см3 готовят электролит необходимой плотности. При двухэтапном процессе степень нагрева раствора серной кислоты будет значительно ниже.
Вначале в ёмкость вливается мерное количество дистиллированной воды, а потом тонкой струёй, при помешивании стеклянной или эбонитовой палочкой, вливается расчетный объем серной кислоты. Кислоту лучше доливать отдельными порциями.
Чтобы приготовить электролит плотностью 1,4 г/см3 из расчета на 1 литр раствора ниже мы приводим таблицу какие пропорции серной кислоты и дистиллированной воды необходимо выдерживать.
Для электролита плотностью 1,4 г/см3 нужно выдерживать пропоции из второй таблицы.
Для приготовлении электролита из плотностью 1,83 г/см3 воспользуйтесь третей таблицей.
Таблица 3
При измерении плотности используют ареометры с пределами измерения 1,1-1,4 г/см3 и ценой деления не грубее 0,005 г/см3 и, поскольку плотность зависит от температуры, термометры на пределы измерения 0÷50С и ценой деления 1С. Термометры не должны иметь деревянных или металлических оправ. Ареометры с указанными пределами измерения и точностью отсутствуют, поэтому применяют набор с более узкими диапазонами измерений.
Как уже упоминалось выше, в процессе приготовления электролита выделяется тепло. В таком случае измерение плотности нагретого электролита будет не корректным, соответственно при измерении необходимо вносить поправку, ну а лучше подождать пока температура станет 20С.
Температурный градиент плотности равен 0,0007 г/см3 на 1С. При температуре электролита выше приведенной, в данном случае 20С, расчетная поправка прибавляется к измеренному значению плотности. Например: температура фактическая равна 30С, разница с приведенной 20С составляет 10С. Градиент 0,0007 х 10 = 0,07 г/см3. К измеренному значению плотности прибавляем поправку, равную 0.007 г/см3.
При фактической температуре 10С разница с приведенной температурой также 10С. Градиент, равный 0,0007 г/см3 умножаем на 10, получаем поправку 0,007 г/см3, но в данном случае поправка вычитается из измеренного значения плотности при температуре 10С.
Использование термина
В естественных науках
Термин электролит широко используется в биологии и медицине. Чаще всего подразумевают водный раствор, содержащий те или иные ионы (напр., «всасывание электролитов» в кишечнике).
В технике
Слово электролит широко используется в науке и технике, в разных отраслях оно может иметь различающийся смысл.
В электрохимии
Многокомпонентный раствор для электроосаждения металлов, а также травления и др. (технический термин, например электролит золочения).
В источниках тока
Электролиты являются важной частью химических источников тока: гальванических элементов и аккумуляторов. Электролит участвует в химических реакциях окисления и восстановления с электродами, благодаря чему возникает ЭДС
В источниках тока электролит может находиться в жидком состоянии (обычно это водный раствор) или загущённым до состояния геля.
Электролитический конденсатор
В электролитических конденсаторах в качестве одной из обкладок используется электролит. В качестве второй обкладки — металлическая фольга (алюминий) или пористый, спечённый из металлических порошков блок (тантал, ниобий). Диэлектриком в таких конденсаторах служит слой оксида самого металла, формируемый химическими методами на поверхности металлической обкладки.
Конденсаторы данного типа, в отличие от других типов, обладают несколькими отличительными особенностями:
- высокая объёмная и весовая удельная ёмкость;
- требование к полярности подключения в цепях постоянного напряжения. Несоблюдение полярности вызывает бурное вскипание электролита, приводящее к механическому разрушению корпуса конденсатора (взрыву);
- значительные утечки и зависимость электрической ёмкости от температуры;
- ограниченный сверху диапазон рабочих частот (типовые значения сотни кГц — десятки МГц в зависимости от номинальной ёмкости и технологии).
Активности в электролитах
Химический потенциал для отдельного i-го иона имеет вид: μi=μi+RTlnai,{\displaystyle \mu _{i}=\mu _{i}^{0}+RTlna_{i},} где ai{\displaystyle a_{i}} — активность i-го иона в растворе.
Для электролита в целом имеем:
μel=∑iviμi=v+μM++v−μA−=v+(μ++RTlnaM+)+v−(μ−+RTlnaA−)={\displaystyle \mu _{el}=\sum _{i}v_{i}\mu _{i}=v_{+}\mu _{M^{+}}+v_{-}\mu _{A^{-}}=v_{+}(\mu _{+}^{0}+RTlna_{M^{+}})+v_{-}(\mu _{-}^{0}+RTlna_{A^{-}})=}
=(v+μ++v−μ−)+RTln(aM+v−⋅aA−v−)=μ+RTlna,{\displaystyle =(v_{+}\mu _{+}^{0}+v_{-}\mu _{-}^{0})+RTln(a_{M^{+}}^{v^{-}}\cdot a_{A^{-}}^{v^{-}})=\mu _{0}+RTlna,} где a{\displaystyle a} — активность электролита; vi{\displaystyle v_{i}} — стехиометрические числа.
Таким образом, имеем:
a=a+v+⋅a−v−.{\displaystyle a=a_{+}^{v^{+}}\cdot a_{-}^{v^{-}}.}
Усредненная активность иона равна:
a±=a+v+⋅a−v−1v++v−.{\displaystyle a_{\pm }=\left^{\frac {1}{v_{+}+v_{-}}}.}
Для одно-одновалентного электролита v+=v−=1{\displaystyle v_{+}=v_{-}=1} и a±=a+⋅a−,{\displaystyle a_{\pm }={\sqrt {a_{+}\cdot a_{-}}},} то есть a±{\displaystyle a_{\pm }} является средним геометрическим активностей отдельных ионов.
Для добавления растворов электролитов принято пользоваться моляльной (m) концентрацией (для водных растворов m численно равен молярной (с) концентрации). Значит, ai=γimi,{\displaystyle a_{i}=\gamma _{i}m_{i},} где γi{\displaystyle \gamma _{i}} — коэффициент активности i-го иона.
Какой должна быть плотность электролита
В традиционных свинцово-кислотных АКБ используют электролит, смешанный в такой пропорции, чтобы его плотность составляла от 1.18 до 1.24 г/см3. Поскольку плотность воды около 1, а серной кислоты – 1.83 г/см3, проще всего готовить раствор поэтапно, особенно если отсутствует ареометр. Сначала жидкости смешивают в одинаковой пропорции, получая раствор ёмкостью около 1.4 г/см3, на втором этапе его уже разводят до нужной консистенции при температуре порядка 20 градусов выше нуля.
Использовать металлические ёмкости для приготовления электролита нельзя (за исключением свинцовых), желательно, чтобы это была фаянсовая, эбонитовая или пластиковая посуда, пластик нужен тоже специальный. Категорически воспрещено использовать стеклянную тару – во время нагрева она может лопнуть.
Измеряют такие свойства электролита аккумуляторов, как плотность, с помощью ареометров, предварительно откалиброванных на значения 1.10–1,45 г/см3 при цене деления шкалы не более 0.005 г/см3. Основная проблема заключается в том, что при изменении температуры меняется и плотность.
А поскольку процедура разбавления воды серной кислотой сопровождается выделением большого количества тепла, для измерения плотности приходится учитывать эти температурные колебания. Для этого используются термометры с ценой деления в один градус, рассчитанные на диапазон 0–50 градусов. К этим измерительным приборам предъявляются такие же требования, как и к ареометрам – они не должны содержать металлических или деревянных частей.
В домашних условиях учитывать температурный фактор гораздо проще, дождавшись, пока после очередного этапа смешивания электролит не остынет до 20º С.
Впрочем, математические выкладки предельно просты: с увеличением температуры на 1 градус плотность жидкости увеличивается на 0.0007 г/см3. То есть, если электролит нагрелся до 30º С, его плотность выросла на 0.007 г/см3.
Напротив, понижение температуры на те же 10 градусов приведёт к уменьшению плотности на такую же величину.
Срок службы
Теперь вы знаете, какую кислоту при производстве и дальнейшем обслуживании добавляют в автомобильный аккумулятор.
Ведётся много споров касательно того, какой эксплуатационный период у раствора. На самом деле срока годности он не имеет. Период службы определяется эффективностью выполняемых функций. Пока электролит справляется со своими задачами, он считается пригодным к использованию.
Срок службы вещества зависит от:
- плотности используемого электролита;
- температуры, в которой эксплуатируется батарея;
- уровня заряда АКБ.
Если поддерживать эти параметры в оптимальных значениях, тогда и кислота будет служить достаточно долго.
Требования к аккумулятору для грузовика, зависимость от объема двигателя
При выборе свинцово-кислотного аккумулятора для грузового автомобиля предъявляются более жесткие требования. Это связано с тем, что ему приходится выдерживать большие стартовые токи и обеспечить запуск двигателей с большим объемом.
При покупке АКБ для грузовика учтите следующие параметры:
Стартовый ток и емкость. Низкий уровень пускового тока может привести к трудностям во время пуска. На этот фактор влияет и емкость аккумулятора. Для грузовиков с бензиновым мотором необходимо учитывать рекомендации производителей. Что касается дизельных моторов, при объеме двигателя от 2,0 до 2,3 л емкость должна быть от 74 до 80 А*ч, а для 2,4-3,0 л и выше — от 80-100 А*ч и более. Помните, чем больше объем мотора, тем выше должна быть емкость аккумулятора.
Долговечность. Этот фактор складывается из нескольких параметров, а именно материала изготовления и условий эксплуатации. Срок службы зависит от правильности применения, наличиях глубоких разрядов и соблюдения других правил (на них остановимся ниже).
Герметичность. Хорошие аккумуляторные батареи должны быть герметичными и выдерживать экстремальные нагрузки в процессе эксплуатации
Желательно, чтобы они сохраняли качества при вибрации и сильных ударах, что особенно важно при установке на грузовых автомобилях. Большой плюс — отсутствие необходимости ухода, а именно контроля уровня электролита, измерения плотности и доливки жидкости.
Напряжение свинцового аккумулятора
В большинстве грузовых автомобилей этот параметр должен составлять 24 Вольта. Но здесь нужно учитывать особенности транспортного средства и модели.
Не менее важный параметр, который нужно учесть при выборе — цена. Стоимость АКБ для грузовика формируется с учетом нескольких параметров: качество свинцового слава, способность к высоким нагрузкам и перепадам температур, производитель и т. д.
Название и роль кислоты электролита
Источник энергии фактически является стандартной батареей. Внутри её находятся анод и катод, а также аккумуляторная жидкость или электролит. Последний представлен раствором кислоты с дистиллированной водой в процентном соотношении 30 к 70, соответственно. Такая пропорция компонентов обеспечивает наиболее эффективное взаимодействие жидкости со свинцовыми пластинами.
Обычная вода содержит примеси, уменьшающие срок службы батареи. А какая кислота в аккумуляторе автомобиля обеспечит появление тока? Та, что вступает в реакции обмена с разными металлами и оксидами, которые необходимы для функционирования батареи. Самым активным из подобных веществ является триоксид серы или ангидрид с химической формулой H2SO4. Более известное и распространённое среди обывателей название — серная кислота.
Когда подключается внешняя нагрузка, тогда взаимодействие жидкости со свинцом и оксидами приводит к необходимым окислительно-восстановительным реакциям. Они противоположны при заряде и разряде батареи. Ток возникает за счёт выделения электронов из свинца положительного элемента, которые принимает оксид отрицательной пластины. А передача заряженных частиц осуществляется благодаря действию раствора, который заливается в батарею.
Основные процессы, протекающие при разряде
На контактах АКБ происходят следующие химические процессы:
- на катоде восстанавливается оксид свинца;
- тратится триоксид серы;
- появляется вода;
- на аноде образуется окись металла.
Получается, что во время реакции кислоту заменяет более лёгкая вода. В результате плотность аккумуляторной жидкости падает. При заряде процессы идут в обратном направлении. После этого под действием возникающего тока начинается электролиз, то есть распад на водород и кислород. Происходит их выделение в газообразной форме. Из-за этого раствор начинает кипеть, так как активно выходят распавшиеся компоненты. Вещества покидают состав смеси, не возвращаясь обратно. Плотность электролита повышается, так как оставшаяся кислота более тяжёлая. Чтобы восстановить первоначальные свойства приходится доливать дистиллированную воду.
Эксплуатация сухозаряженного автомобильного аккумулятора
После проведения мероприятий по подготовке аккумулятора этой разновидности к работе, он превращается в обычный свинцово-кислотный обслуживаемого типа. Следовательно, основные эксплуатационные правила остаются:
- Стараться не допускать полного разряда АКБ.
- По возможности не осуществлять зарядку высокими токами или делать это лишь в исключительных случаях.
- Регулярно контролировать уровень электролитной жидкости и её плотность, не допуская «оголения» банок (поверхность электродов вне жидкой среды подвержена ускоренной сульфатации).
- Необходимо помнить о том, что в летнюю жару и зимний холод поездки на короткие расстояния негативным образом сказываются на сроке службы.
- Следить за отсутствием белесоватых подтёков на корпусе.
- Протирать поверхность батареи, удаляя с неё пыль и грязь.
Как поднять плотность электролита
Кислотность электролита можно поднять двумя способами: полной заменой старого электролита на новый или внесением разбавленной концентрированной кислоты.
В случае разбавления жидкости следует провести ряд действий для каждой банки:
При замере плотности стоит определить необходимый уровень. Если не произошло изменений, тогда в половину оставшегося объема требуется внести еще электролит.
С помощью подобных манипуляций можно довести до оптимальной плотности концентрацию кислоты в электролите.
Важно! Серная кислота – агрессивная средой для кожных покровов человека и его одежды. Поэтому во время работ с открытой батареей рекомендуется позаботиться о мерах защиты: обязательно надеть резиновые перчатки, защитные очки
Так же пригодится прорезиненный фартук.
Как правильно заливать и доливать раствор
Особой потребности отдельно приобретать серную кислоту и дистиллированную воду не обязательно. Последняя находится в свободной продаже, в то время как кислоты заполучить намного сложнее.
Поэтому для автомобилистов просто продают уже готовые растворы электролита. Их смешивают в соответствующих пропорциях, и получают составы для разных ситуаций и времени года. К примеру, для получения электролита плотностью 1,29 г/см3, на 1 литр дистиллята добавляется 360 мл. кислоты. То есть здесь соотношение составляет 1 к 3.
Это потенциально очень опасно для человека. Поэтому запомните, что только в воду добавляется кислота, а не наоборот.
Сам же процесс заливки и доливки выглядит следующим образом:
- Заливать или доливать электролит рекомендуется с помощью полиэтиленовой или стеклянной трубки.
- Уровень вещества в аккумуляторе автомобиля должен находиться в пределах от 10 до 15 мм над пластинами из свинца.
- Добавив необходимое количество раствора, аккумулятор стоит оставить в покое примерно на 2 часа. Но бывает так, что за это время плотность успевает упасть.
- Затем аккумулятор следует зарядить током. Его значение должно быть в 10 раз меньше, чем ёмкость батареи.
- Зарядка на низком токе продолжается в течение 4 часов.
С целью профилактики и поддержания оптимального состояния, проверка плотности проводится с интервалом в 2-3 месяца. Минимум 3-4 раза в год этот показатель нужно обязательно проверять. Сделать это можно с помощью ареометра.
Разновидности
Опираясь на основные характеристики, актуальные для свинцово-кислотных аккумуляторов, их можно разделить на соответствующие подкатегории.
Для начала стоит акцентировать внимание на возможностях их обслуживания. Тут выделяют такие типы свинцово-кислотных питающих аккумуляторов:
- Обслуживаемые. Предусматривают наличие открытой конструкции. То есть корпус не герметичный. Производитель устанавливает специальные съёмные крышки, позволяющие получить доступ к банкам. Тем самым можно по мере необходимости доливать электролит или кислоту, визуально проверять уровень жидкости и состояние пластин, делать замеры плотности ареометром.
- Необслуживаемые. Корпус полностью герметичный. Обслуживание сводится только к контролю заряда с помощью индикатора, а также подключению АКБ к зарядному устройству.
Популярность вторых вполне очевидна. Обслуживаемые АКБ встречаются всё реже, поскольку технологии совершенствуются, от автомобилистов требуется меньше усилий и внимания для поддержания аккумулятора в рабочем состоянии.
Опираясь на такие основные характеристики как назначение и область применения, выделяют следующие разновидности свинцово-кислотных аккумуляторов.
- Стартерные АКБ. Могут за короткое время выдать большое количество энергии. Из-за этого обладают большим саморазрядом. Необходимые для автомобилей виды батарей. Нуждаются в вентиляции и определённом обслуживании.
- Буферные. Такие виды свинцово-кислотных питающих аккумуляторов служат для того, чтобы в течение небольшого времени хранить сравнительно малый объём энергии. Они функционируют в режиме постоянной подзарядки.
- Для бесперебойных устройств. Чаще всего можно встретить в офисах, предназначаются для компьютерной техники. При возникновении перебоя с электроэнергией позволяют без потери данных успеть завершить работу.
- Для длительного снабжения энергией. Отличаются большим весом и габаритами. Но это позволяет питать потребителей долгое время. Подобные решения можно встретить в медицинской сфере, в отделениях реанимации. Могут питать достаточно внушительное количество потребителей длительное время.
- Гелевые. Существует 2 основных технологии производства гелевых АКБ. Это AGM и GEL. Характеризуются гелеобразным состоянием электролита. Усовершенствованная технология, хотя в её основе всё равно лежат свинец и серная кислота. Гелевые АКБ применяются в автомобилях, используются для работы солнечных батарей и пр.
Чтобы получить определённые характеристики, вносятся соответствующие изменения в конструкцию.
Когда нужно отдать много энергии за короткое время, пластины делают тонкими, но высокими и широкими, уменьшая между ними расстояние. Это позволяет им быстрее отдавать энергию.
Если потребляется мало энергии, но долго, тогда пластины должны быть толстыми, короткими и узкими, расстояние между ними увеличивают.
На параметры АКБ влияют также электролит, применяемые легирующие добавки, такие как кальций, серебро, цинк и пр. Это позволяет выделять ещё несколько разновидностей. Часто встречаются свинцово-кальциевые АКБ.
Контроль плотности
Плотность в автомобильном свинцово-кислотном аккумуляторе измеряют в гр/см³, и она должна быть пропорциональна концентрации раствора с обратной зависимостью температур жидкости. Нормальный показатель — 1,27-1,29 гр/см³. Этот показатель позволяет определить состояние батареи, и если она не держит заряда, то необходимо проверить количество вещества. Со временем уровень электролита аккумулятора автомобиля сокращается, и соответственно, увеличивается плотность при гидролизе воды и нагрева. Для этого требуется периодически доливать дистиллированную воду, снижая концентрацию серной кислоты. Процедуру можно выполнить самостоятельно, если знать, сколько требуется для определенной модели вещества.

Электролит для аккумуляторов можно приобрести в магазинах, либо сделать своими руками и научиться регулировать плотность, своевременно измерять и ухаживать за устройством для продления срока службы.
Для приготовления потребуются следующие компоненты:
- Серная кислота.
- Вода дистиллированная.
- Емкость из стекла, свинца, керамики, устойчивая к воздействию химического вещества.
- Эбонитовая баночка для размешивания.
Для приготовления в емкость заливается дистиллированная вода, затем серная кислота, и палочкой параллельно помешивается получаемая смесь. Процедуру проводят последовательно, так как при обратном варианте можно получить ожоги. Если места эксплуатации автотранспорта климат умеренный, то следует придерживаться такой пропорции веществ: на 1 л воды — 0,36 л кислоты. Для теплого климата на 1 л воды следует заливать кислоту в объеме 0,33 л. Полученное вещество накрывается и оставляется на сутки до образования осадков и остывания. При замене электролита в аккумуляторе надевают резиновые перчатки и очки для защиты глаз.
Напомним, что при обратном проведении заливки, в частности, первой воды, возможна реакция гидратации и образования тепла в кислоте. Вероятно, что вода закипит и спровоцирует разбрызгивание.
Проверять плотность аккумулятора необходимо раз в три месяца. Для этого пользуются ареометром.
Повышение плотности электролита
Если текущая плотность используемой кислоты в аккумуляторе автомобиля очень высокая, тогда достаточно добавить в банки воды, и показатели будут оптимизированы.
Но в обратном направлении этот приём не работает. Добавляя воду, увеличить кислотность точно не получится.
Объяснить это просто. По завершению окислительно-восстановительных реакций вода может распадаться и теряться. Из-за этого концентрация кислоты будет увеличиваться. Используя зарядные устройства, можно компенсировать недостаточную плотность. Если этот метод не помогает, тогда в батарею требуется залить электролит корректирующего типа.
На практике концентрация обычно повышается путём полной замены электролита либо же за счёт добавления разбавленной кислоты.
Используя метод разбавления, нужно выполнить такие операции, причём для каждой банки аккумуляторной батареи:
- С помощью шприца или медицинской груши постепенно откачать максимально возможное количество жидкости.
- Добавить в банку половину её объёма разбавленную концентрированную кислоту с плотностью около 1,26-1,28 г/см3.
- Подать нагрузку на выводы с минимальной мощностью, что позволит тщательно перемешать компоненты.
Замеряя плотность, не забывайте проверять уровень. Если после проведённых манипуляций никаких изменений не наблюдается, тогда добавляется ещё часть электролита. Постепенно контролируя параметры аккумулятора, создаются оптимальные значения концентрации.
Если при проверке плотности обнаруживаются значения ниже 1,2 г/см3, тогда выход только один. Это полная замена электролита, поскольку путём разбавления повысить уровень до нужных значений уже не получится.
В процессе работы нужно обязательно предварительно подумать о средствах защиты. Работать с электролитом лучше в резиновых перчатках, очках и в прорезиненном фартуке.

Физические свойства сернокислотного электролита
Есть еще один физический фактор, который необходимо учитывать, особенно когда приготавливаются большие объемы раствора серной кислоты и дистиллированной воды. Это то обстоятельство, что при смешивании равных объемов серной кислоты и воды, после охлаждении такого раствора его объем будет меньше, чем сумма первоначальных объёмов. Что бы учесть этот фактор нужно обратится к четвертой таблице, в которой указаны величины уменьшения объёмов для растворов серной кислоты различной плотности.
Вязкость
Вязкость это свойство электролита, наиболее существенно влияющее на работоспособность свинцового аккумулятора. Электрохимические процессы, протекающие при работе аккумулятора, носят диффузионный характер. Скорость диффузии, в основном, зависит от вязкости электролита. Именно скоростью диффузии определяется поступление электролита к поверхности и в поры электродов при разряде, особенно при установке жестких (минутных, часовых) режимов разряда.
Чем вязкость выше, тем диффузия медленнее. При понижении температуры на 25С вязкость электролита возрастает в 2 раза, а при температуре в -50С она возрастает почти в 30 раз по сравнению с вязкостью при нормальной температуре. С увеличением вязкости падает ёмкость. Именно поэтому ра6отоспособность свинцовых аккумуляторов при низких температурах ухудшается. Это обстоятельство необходимо учитывать при установке герметичных аккумуляторов с гелевым (загущённым) электролитом.
Удельное сопротивление электролита
Сопротивление электролита, занимающего объем, ограниченный длиной 1 см и сечением в 1 см3, рассчитывается по формуле:
=rS/L
где r – удельное сопротивление Ом см;
L- длина, см.
S — поперечное сечение см2.
Сопротивление изменяется с изменением концентрации и температуры электролита.
Чтобы иметь минимальное внутреннее сопротивление АКБ, желательно применять электролит с наименьшим удельным сопротивлением.
Величины удельных сопротивлений приведены в таблице 5.
Таблица 5. Удельные сопротивления электролита
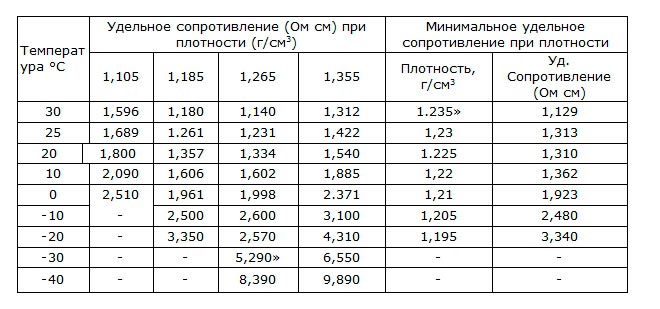
Удельное сопротивление электролита возрастает при снижении температуры, наиболее значительно при температуре 0С.
Температура замерзания электролита важна, постольку по мере разряда аккумулятора снижается его плотность и, соответственно, температура его замерзания. При замерзании объем электролита увеличивается, что приводит к разрушению сосуда и электродов аккумулятора. Наиболее низкую температуру замерзания имеет электролит плотностью 1,29 г/см3. Стартерные аккумуляторные батареи, эксплуатируемые в суровых условиях, имеют электролит плотностью 1,26-1,30 г/см3, который не замеряет при самых низких возможных температурах.
Для определения температур замерзания электролитов различной плотности следует пользоваться таблицей 6.
Используемый вид кислоты
Автомобилистов закономерно интересует, какие кислоты используются в аккумуляторах автомобилей. В действительности существуют разные варианты и догадки на этот счёт.
Некоторые уверены, что здесь применяется только соляная кислота. Другие делают ставки на серную.

Поэтому важно ответить, какая именно кислота находится в аккумуляторе, серная или же соляная. Запомните раз и навсегда
В АКБ применяют только серную кислоту
Запомните раз и навсегда. В АКБ применяют только серную кислоту.
Если вас когда-то спросят, какая кислота всегда находится в аккумуляторе, смело отвечайте, что серная. Но никак не соляная. Это распространённое заблуждение.
Также будет полезно знать, как ещё называется кислота, используемая в аккумуляторе. Да, чаще всего её называют просто серной. Но есть и другое название. А именно триоксид серы или ангидрид серы. Сами понимаете, что понятие серной кислоты запомнить намного проще.
Определившись с тем, какая кислота всегда заливается в автомобильный аккумулятор, можно рассказать о ней некоторые подробности, а также взглянуть на особенности готового к использованию электролита.
Вообще различают несколько видов аккумуляторов, и не всегда есть смысл спрашивать, какую кислоту в их случае добавляют, поскольку аккумулятор определённого типа не предусматривает её применение. Это те же литиевые АКБ и никель-кадмиевые. В последнем случае вместо кислоты применяется щёлочь.
Несколько иначе обстоят дела с гелевыми АКБ. Если говорить о том, какую кислоту всегда добавляют в такой аккумулятор, то тут ответ будет аналогичным. Кислота там серная. Только находится электролит в гелеобразном состоянии.
Подавляющее большинство АКБ, применяемых в авто, являются свинцово-кислотными. Они делятся на несколько разновидностей, в зависимости от добавок и агрегатного состояния электролита. Но практически всегда речь идёт именно о кислотных устройствах. И вы теперь знаете, какая кислота применяется в АКБ.
Пропорции раствора примерно всегда одинаковые. Это от 30 до 35% кислоты, всё остальное занимает вода.
Крайне редко процентное соотношение превышает 35 на 65%. Чтобы выполнять все задачи, поставленные перед автомобильными АКБ, вполне достаточно и 30%.
Теперь вы знаете, какая именно кислота всегда находится в автомобильном аккумуляторе. Это позволит понять, что необходимо покупать для последующего обслуживания.
Смысл обслуживания заключается в том, чтобы добавлять определённое количество готового электролита либо же только дистиллированную воду.
Но объективно мало просто понимать, какая кислота обычно при производстве используется в аккумуляторе того или иного автомобиля. Предстоит ещё немного разобраться с понятиями концентрации и плотности.